inštrukcije > kemija > Poimenovanje anorganskih spojin
Objavljeno: 24.4.2019
Element je osnovni gradnik spojin. Je čista snov, ki se je z kemijskimi reakcijami ne da razbiti še na enostavnejše snovi. Vsak element ima svoje ime in svoj simbol, ki je sestavljen iz ene ali dveh črk. V dvočrkovnih elementih je prva črka vedno velika, druga pa majhna.
Izvor imen elementov je različen. Poimenovani so po geografskih imenih (francij, americij), po znanstvenikih (mendelevij, nobelij), po mitoloških bitjih (titan, niobij) ali po planetih (uran, plutonij).
Veliko elementov je tudi poimenovanih v latinščini in iz latinskih imen so izpeljani tudi njihovi simboli. Kor primer je vodik, katerega simbol H izvira iz latinske besede hydrogenium, ali zlato, katerega simbol Au izvira iz latinske besede aurum.
Binarne spojine so spojine, ki so sestavljene iz dveh različnih elementov. Za poimenovanje spojin imamo posebna pravila, katerih skupek teh imenujemo kemijska nomenklatura.
Binarne spojine lahko poimenujemo na dva načina – z grškimi števniki in po Stockovemu sistemu.
Pri poimenovanju grških števnikov navedemo število atomov in ime elementa. Uporabljamo grške števnike di (2), tri (3), tetra (4), penta (5), heksa (6), hepta (7), okta (8), nona (9) in deka (10).
Imena nekaterih spojin so izražena v latinskih imenih. Zbrane so v spodnji tabeli:
Oglejmo si nekaj primerov spojin:

K prvemu elementu v spojini, ki se poimenuje s slovenskim imenom, dodamo končnico -ev ali -ov, zadnjemu elementu pa k latinskemu imenu dodamo končnico -id. Nato še pred imenom elementov, ki jih je v spojini več kot dva, dodamo grške števnike.
Imenovanje po Stockovem sistemu je podobno, le da namesto grških števnikov navedemo oksidacijsko število bolj pozitivnega elementa. Oksidacijsko število je naboj, ki bi ga imel atom v molekuli, če bi bila ta zgrajena zgolj iz ionov. Zapisujemo ga nad simbolom elementa. Najprej navedemo predznak (+ ali −), nato pa še številčno vrednost. Isti element ima v različnih spojinah lahko različna oksidacijska števila. V binarnih spojinah ima levo zapisani element običajno pozitivno, desno zapisani element pa običajno negativno oksidacijsko število.
Pri določanju oksidacijskih števil si pomagamo z naslednjimi pravili:
• vsota oksidacijskih števil vseh elementov v spojini je 0,
• vodik ima oksidacijsko število +1 ali −1,
• kovine prve skupine periodnega sistema imajo oksidacijsko število +1, druge skupine +2, kovine tretje skupine pa običajno +3,
• kot negativni deli spojin (zapisani desno) imajo elementi sedme skupine periodnega sistema oksidacijsko število −1, elementi šeste skupine −2, elementi pete skupine pa −3.
Spojine iz prejšnjega primera poimenujmo še po Stocku. Najprej poimenujemo prvo ime elementa s slovenskim imenom in mu pripišemo končnico -ov ali -ev. Nato dodamo v oklepajih rimsko število, ki nam ponazarja naboj pozitivnega iona v spojini, na koncu pa latinsko ime spojine z končnico -id.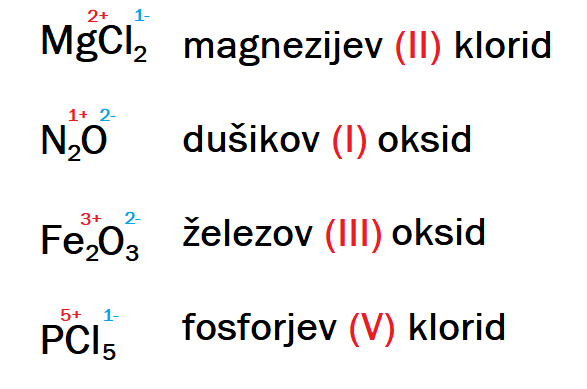
Klor in kisik imata fiksni oksidacijski števili 1- in 2-. Ker sta v prvi spojini 2 atoma klora z oksidacijskim številom 1-, bo oksidacijsko število magnezija 2+. V drugi spojini sta dva atoma dušika, zato bo oksidacijsko število 1+. V tretji spojini so trije atomi kisika z oksidacijskim številom 2-, skupni naboj teh je 6- in dva atoma železa. Ker želimo naboje izenačiti, delimo izračunan skupni naboj z dvema atomoma dušika in tako dobimo naboj dušika, ki je 3+. V četrti spojini je pet atomov klora z oksidacijskim številom 1- ter en atom fosforja, zato bo oksidacijsko število tega 5+.
Binarne kisline so kisline, ki po navadi vsebujejo vodik in še eno nekovino. Najbolj znane binarne kisline so vodikovi halogenidi, to so vodikov fluorid (HF), vodikov klorid (HCl), vodikov bromid (HBr) in vodikov jodid (HI). Vse spojine se pojavljajo kot plini, raztopine le teh pa imenujemo fluorovodikova, klorovodikova in bromovodikova kislina.
Poznamo še spojini vodikov sulfid, H2S, pri katerem pa števnik di- izpustimo, in vodikov cianid HCN. Raztopini le teh imenujemo žveplovodikova in cianovodikova kislina.
Oksokisline so kisline, ki poleg vodika in značilne nekovine vsebujejo tudi kisik. V formulah teh snovi zapisujemo elemente po naslednjem vrstnem redu: vodik–značilna nekovina–kisik.
V imenu oksokisline navedemo značilno nekovino in njeno oksidacijsko število. Vodikovih in kisikovih atomov ne navajamo. Oksidacijsko število nekovine v oksokislini dobimo z izenačenjem vsote skupnih nabojev vodika in kisika in ga v imenu pišemo po Stockovemu sistemu.
Najbolj znana oksokislina je žveplova (VI) kislina, H2SO4. Ima štiri atome kisika z oksidacijskim številom 2-, skupni naboj kisikov je 8-, ter dva atoma vodika z nabojem 1+, skupni naboj vodikov je 2+. Če seštejemo oba skupna naboja, dobimo 6-. Da v oksokislini izenačimo naboje, mora nekovina imeti naboj 6+, zato je ime spojine žveplova (VI) kislina.
Drug znan primer je fosforjeva (V) kislina, H3PO4. Ima štiri atome kisika z nabojem -2, skupni naboj teh kisikov je 8-, ter tri atome vodika z nabojem 1+, katerih je skupni naboj 3+. Seštevek vseh nabojev je 5-, zato mora biti naboj v fosforju 5+, da naboje med sabo izenačimo. Ime spojine je fosforjeva (V) kislina.
Lotili se bomo še zadnjega primera, to je ogljikova (IV) kislina, H2CO3. Ima tri atome kisika z nabojem -2, skupni naboj teh kisikov je 6-, ter dva atoma vodika z nabojem 1+, katerih je skupni naboj 2+. Seštevek vseh nabojev je 4-, zato mora biti naboj v ogljiku 4+. da naboje med sabo izenačimo. Ime spojine je ogljikova (IV) kislina.
Za vajo ostale primere ugotovite naboje sami.
Baze so kovinski hidroksidi. Poimenujemo jih tako, da k kovini dodamo končnico –ov ali –ev in zraven pripišemo hidroksid. Najbolj znani spojini sta natrijev in kalcijev hidroksid. Amonijak NH3 je tudi baza, raztopina tega se imenuje amonijev hidroksid. Oksidacijsko število hidroksidnega iona je vedno 1-. Negativni naboj se navezuje na celoten hidroksidni ion, zato je ta označen z rdečo črto.
Poimenovanje soli je podobno kot poimenovanje kislin, izjeme so kristalohidrati.
Najbolj znan predstavnik te skupine je natrijev klorid, oz. navadna kuhinjska sol. V molekuli je po en atom vsakega atoma, kajti obe oksidacijski števili se med seboj izenačita. Drugače je pri kalcijevem kloridu, kjer ima kalcij naboj 2+, klor pa samo 1-, zato potrebujemo dva atoma klora, da naboje izenačimo. Cianidi so še ena izmed posebnih skupin soli, naboj cianidnega iona, CN- je 1-. Zato v molekuli kalcijevega cianida tudi potrebujemo dva cianidna iona, da izenačimo naboj. Naboj amonijevega iona je 1+, zato je za izenačitev naboja dovolj en atom klora.
Soli oksokislin so ponavadi derivati kovinskih hidroksidov in oksokislin. Za razliko od kislin rimsko številko v oklepaju pišemo na koncu imena. Soli oksokislin vsebujejo sledeče ione: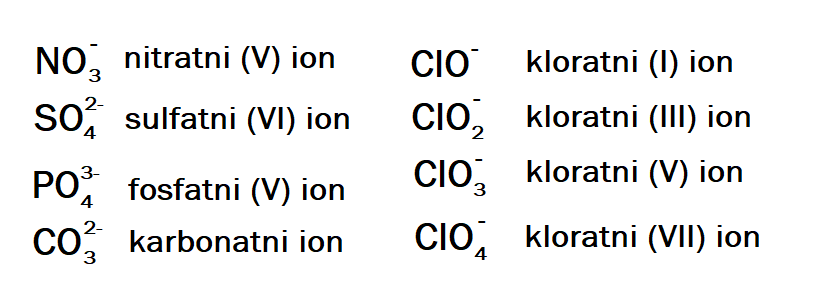

Na sledečih primerih bomo zapisali formule in imena soli oksokislin. V prvi molekuli imamo sulfatni (VI) ion z nabojem 2- in natrijev ion z nabojem 1+, zato potrebujemo 2 atoma natrija. Ime spojine je natrijev sulfat (VI). V drugem primeru se naboja v obeh ionih med sabo izenačita, zato je potreben samo eden izmed njiju. Ime spojine je kalcijev sulfat (VI), kajti ta vsebuje sulfatni (VI) ion. Pri tretjem primeru je naboj fosfatnega (V) iona 3-, kalcijevega pa 2+. Če želimo izenačiti naboj, potrebujemo tri atome kalcija in dva fosfatna (V) iona. Če ima sol oksokislin več kislinskih ionov, se ti pišejo v oklepaju in zadaj pripišemo število. Ime spojine je pa kalcijev (V) fosfat.
Kristalohidrati so spojine, ki imajo nase kristalno vezane molekule vode. Poimenujemo jih tako, da imenu spojine dodamo grški števnik, ki označuje število molekul vode in nato dodamo besedo hidrat.
Najbolj znani primer kristalohidrata je modra galica. Bakrov in sulfatni (VI) ion sta v spojini v razmerju 1:1, kajti njuna naboja se med sabo izenačita. Kristalohidrat ima nase vezanih 5 molekul vode, zato mu pripišemo besedo pentahidrat. Končno ime spojine je bakrov(II) sulfat(VI) pentahidrat.
Potrebujete dodatne informacije? Pomagajo vam lahko inštruktorji kemije.
kemija
Določite lokacijo
Določite termin
Dodatni filtri
Počisti
OŠ/SŠ
Študenti in ostali
Poišči mojo
lokacijo
Na domu
Online
Danes
(cena +50%)
Jutri
Jutri popoldne
Pojutrišnjem
Pojutrišnjem popoldne
Ta teden
Ta teden popoldne
V naslednjih treh dneh
V naslednjih treh dneh popoldne
Kadarkoli
Cena
Spol
Starost
Fakulteta
Razvrsti po:
Razvrsti po:


Zapri okno