inštrukcije > kemija > Molekulske kemijske vezi
Objavljeno: 13.3.2019
Z molekulskimi ali van der Waalsovimi vezmi (imenovane po nizozemskem fiziku Johannesu D. van der Walsu) opisujemo privlačne sile, ki delujejo med molekulami oz. med nasprotnimi poli molekul (pozitivni pol ene molekule se z električno silo privlači z negativnim polom druge molekule).
Te vezi so bistveno šibkejše kot ionske in kovalentne. Vezi pa so neusmerjene.
Vrste molekulskih sil (vezi):
Delujejo na zelo kratki razdalji. Nastanek teh vezi, pa je posledica elektrostatične privlačnost med nasprotnima nabojema.
Orientacijska sila se pojavlja med polarnimi molekulami. Za polarne molkekule pa je značilno, da imajo stalen dipol.
Pri približevanju na dovolj majhne razdalje se molekule orientirajo (od tu ime orientacijske vezi) tako, da se negativen del ene molekule usmeri k pozitivnemu delu druge molekule.
Jakost je odvisna od polarnosti molekul-bolj polarne tvorijo močnejše vezi.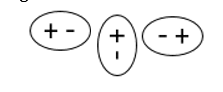
Indukcijska sila se pojavlja se med polarno in nepolarno molekulo.
Jakost je odvisna od polarnosti polarne molekule (vrednosti dipolnega momenta) in od molske mase/št. elektronov nepolarne molekule. Čim večja molska masa oz. čim več elektronov ima nepolarna molekula lažje se polarizira.
Polarna molekula povzroči polarizacijo nepolarne molekule-inducira kratkotrajen dipol (od tu ime indukcijske sile). Torej govorimo o privlačni sili med stalnim in kratkotrajnim dipolom.
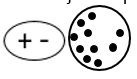
Disperzijska sila je najšibkejša od med molekulskih sil. Pojavlja se med nepolarnimi molekulami.
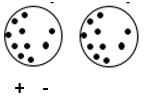
Elektroni v molekuli oz. v atomu se ves čas gibajo, v določenem trenutku ima molekula oz. atom več elektronov na eni strani kot na drugi in, ko se taki molekuli oz. atomu približa druga taka molekula pride do premika elektronov in s tem do elektrostatskega privlaka.
Jakost je odvisna od molekulske mase oz. št. elektronov.
DODATNO: Zaradi teh sil se žlahtni plini lahko utekočinijo.
Vodikova vez je po značilnostih drugačna od Van der Waalsovih sil.
Je močnejša od Van der Waalsovih sil in šibkejša od medatomskih vezi.
Je usmerjena.
Za vodikovo vez velja, da nastane med delno pozitivnim vodikom v eni molekuli in delno negativnim atomom v drugi molekuli.
Pomen vodikove vezi (primeri):
Vodikova vez povezuje dvojno vijačnico nukleinskih kislin in nastopa med verigami beljakovin.
Primer je voda. V strukturi ledu so vse vezi med seboj povezane z vodikovimi vezmi (glej sliko). Pri tej vezavi nastanejo praznine in zato led plava na vodi.
Druge posledice vodikove vezi pri vodi:

Vaje:
Ponovitev: medatomske vezi
V kateri snovi so molekule med seboj povezane z vodikovimi vezmi?
a) vodik
b) fluorometan
c) aceton
d) metanol
Opredeli molekulsko silo (vez), ki prevladuje med:
a) molekulami HI, orientacijske vezi
b) med molkekulami Br2 in molekulami H20, indukcijske vezi
c) molekulami H2O2, vodikova vez
d) molekulami N2, disperzijska vez
Potrebujete dodatne informacije? Pomagajo vam lahko inštruktorji kemije.
kemija
Določite lokacijo
Določite termin
Dodatni filtri
Počisti
OŠ/SŠ
Študenti in ostali
Poišči mojo
lokacijo
Na domu
Online
Danes
(cena +50%)
Jutri
Jutri popoldne
Pojutrišnjem
Pojutrišnjem popoldne
Ta teden
Ta teden popoldne
V naslednjih treh dneh
V naslednjih treh dneh popoldne
Kadarkoli
Cena
Spol
Starost
Fakulteta
Razvrsti po:
Razvrsti po:


Zapri okno