inštrukcije > kemija > Kemijsko ravnotežje
Objavljeno: 17.7.2019
Poznamo dva tipa reakcij:
Enosmerne (=nepovratne) reakcije so tiste, ki potekajo v eni smeri-reaktanti se pretvorijo v produkte. Pri pisanju enosmernih reakciji uporabljamo enosmerno puščico. Reakcije potekajo dokler ne zmanjka produktov.
A + B —> C + D
v=k[A][B]
Primer: Mg + 2HCl —> MgCl2 + H2
v=k[Mg][HCl]
Ravnotežne reakcije so reakcije pri katerih se del reaktantov pretvori v produkte na kar se med reaktanti in produkti vzpostavi dinamično ravnotežje. To je stanje ravnotežnega sistema v katerem sta hitrosti kemijskih sprememb v obeh smereh enaki.
V1=V2
Dinamično ravnotežje
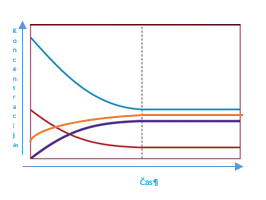
Na grafu koncentracija v odvisnosti od časa sta z svetlo modro in rdečo krivuljo zarisani spremembi koncentracije reaktantov. Z oranžno in s temno modro pa sta zarisani krivulji produktov. Levo od črtkane črte se koncentracija ne spreminja več. Pravimo, da je stalna.
Ravnotežje delimo na dve vrsti-glede na to v kakšnem agregatnem stanju so snovi.
Če so v istem agregatnem stanju je to homogeno ravnotežje
Primer: 2SO2 (g) + O2(g) ⇌ 2SO3(g)
Če so v različnem agregatnem stanju je to heterogeno ravnotežje
Primer: CaCO3(s) ⇌ CaO(s) + CO2(g)
Ravnotežna konstanta (Kc) predstavlja razmerje med množinskimi koncentracijami produktov in reaktantov.
Kc > 1 prevlada produktov
Kc < 1 prevlada reaktantov
Za reakcijo aA + bB ⇌ cC + dD, kjer so a, b, c in d koeficienti urejene enačbe, zapišemo konstanto ravnotežja: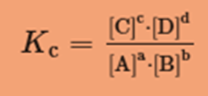
Naloga uredi kemijsko enačbo in določi konstanto ravnotežja: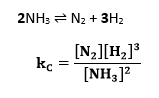
Zgled težje naloge: Na začetku imamo 4 mol ogljikovega monoksida in 3,4 mol vode. Zanima nas kolikšna je koncentracija CO2, če nastane 2,2 mol vodika.
V prvem delu naloge uredimo kemijsko reakcijo in izpišemo podatke.
CO + H20 ⇌ CO2 + H2
n(CO)= 4 mol
n(H2O)= 3,4 mol
n(H2) = 2,2 mol
V= 1 L
V drugem delu vaje ustvarimo tabelo tako, da prepišemo reaktante in produkte v zgornjo vrstico tabele. Na skrajno desno stran vpišemo začetek, potek in ravnotežje.
V tretjem delu vaje izpolnimo tabelo. Ker nas naloga sprašuje po koncentracijah v tabelo vpisujemo koncentracije.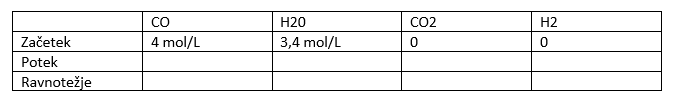
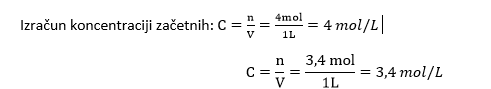
Na začetku produktov nimamo. Zato v zgornjo vrstico pri produktih zapišemo 0.


Ta del enačbe med seboj enačimo, da dobimo neznanko x.
0+x=2,2 mol/L x=2,2mol/L
Zdaj lahko do konca izpolnimo tabelo. Na mesto x vstavimo 2,2 mol/l.
Ravnotežni sistem se odzove na spremembo temperature, tlaka in koncentracij snovi, ki sodelujejo v kemijskem ravnotežju.
Temperatura: Pri povišanju temperature se ravnotežje pomakne v smer endotermne reakcije. Pri znižanju temperature pa v smeri eksotermne reakcije.
Tlak: Pri povišanju tlaka (ali zmanjšanju volumna) se ravnotežje pomakne v smeri nastanka manjšega števila molekul, pri znižanju tlaka (zvišanju volumna) pa v smeri večjega števila molekul.
Koncentracija: Pri povečanju koncentracije reaktantov ali zmanjšanju koncentracije produktov se ravnotežje pomakne v smeri produktov. Pri zmanjšanju koncentracije reaktantov ali povečanju koncentracije produktov se ravnotežje pomakne v smeri reaktantov.
Naloga: Kam se premakne kemijsko ravnotežje?
PCl5 ⇌ PCl3 + Cl2 (∆Hr > O)
a) Povečamo temperaturo —>
b) Zmanjšamo tlak —>
c) Povečamo volumen —>
č) Povečamo koncentracijo PCl5 —>
d) Zmanjšamo koncentracijo PCl5 <—
e) Dodamo katalizator Ni spremembe
Nadaljevanje razlage: Protolitske reakcije
Potrebujete dodatne informacije? Pomagajo vam lahko inštruktorji kemije.
kemija
Določite lokacijo
Določite termin
Dodatni filtri
Počisti
OŠ/SŠ
Študenti in ostali
Poišči mojo
lokacijo
Na domu
Online
Danes
(cena +50%)
Jutri
Jutri popoldne
Pojutrišnjem
Pojutrišnjem popoldne
Ta teden
Ta teden popoldne
V naslednjih treh dneh
V naslednjih treh dneh popoldne
Kadarkoli
Cena
Spol
Starost
Fakulteta
Razvrsti po:
Razvrsti po:


Zapri okno