inštrukcije > kemija > Hitrost kemijske reakcije
Objavljeno: 10.3.2019
Kemijske reakcije lahko potekajo različno hitro, nekatere počasneje, nekatere pa hitreje. Kemijska kinetika je panoga, ki proučuje hitrosti in mehanizme kemijske reakcije ter vplive na hitrost kemijske reakcije.
Pri kemijski reakciji se reaktanti porabljajo in pri tem nastajajo produkti. Koncentracije reaktantov se zmanjšujejo in koncentracije produktov se povečujejo. Hitrost kemijske reakcije izrazimo s spremembo množinske koncentracije snovi reaktanta ali produkta v določeni časovni enoti.
Enačbi hitrosti reakcije za pretvorbo reaktanta A v produkt B (A → B):
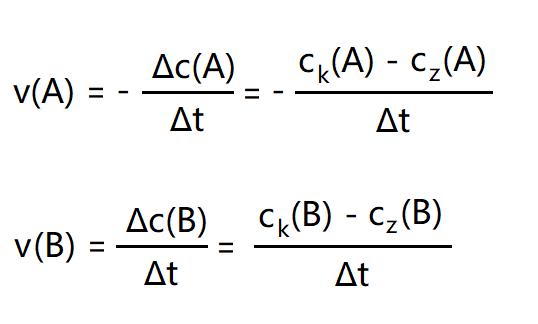
v(A) – hitrost spremembe koncentracije reaktanta A [mol/Ls]
v(B) – hitrost spremembe koncentracije produkta B [mol/Ls]
∆c – sprememba množinske koncentracije [mol/L]
ck – množinska koncentracija snovi na koncu časovnega intervala (končna množinska koncentracija) [mol/L]
cz – množinska koncentracija snovi na začetku časovnega intervala (začetna množinska koncentracija) [mol/L]
∆ t – časovni interval [s]
Enostavna formula za zapis hitrosti kemijske reakcije reaktanta in produkta se glasi: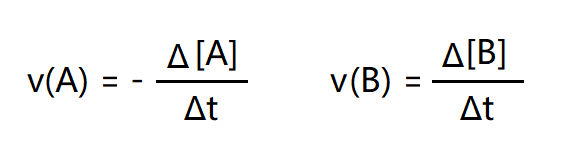
Hitrost kemijske reakcije izražamo s spremembo množinske koncentracije snovi v časovni enoti. Enačba hitrosti glede na reaktant ima negativni predznak, ker se koncentracija reaktanta tekom reakcije zmanjšuje. Tako ima izračunana hitrost vedno pozitivno vrednost.
Hitrost kemijske reakcije se tekom reakcije spreminja. Na začetku je hitrost reakcije običajno največja, nato pa se postopoma zmanjšuje do porabe reaktantov oz. do vzpostavitve ravnotežja med reaktanti in produkti. Zato običajno ugotavljamo povprečno hitrost reakcije v določenem časovnem intervalu. Hitrost reakcije ugotovimo tako, da merimo koncentracijo določene snovi v posameznem časovnem intervalu in nato razliko med izmerjenima koncentracijama snovi delimo s časom, v katerem je prišlo do spremembe.
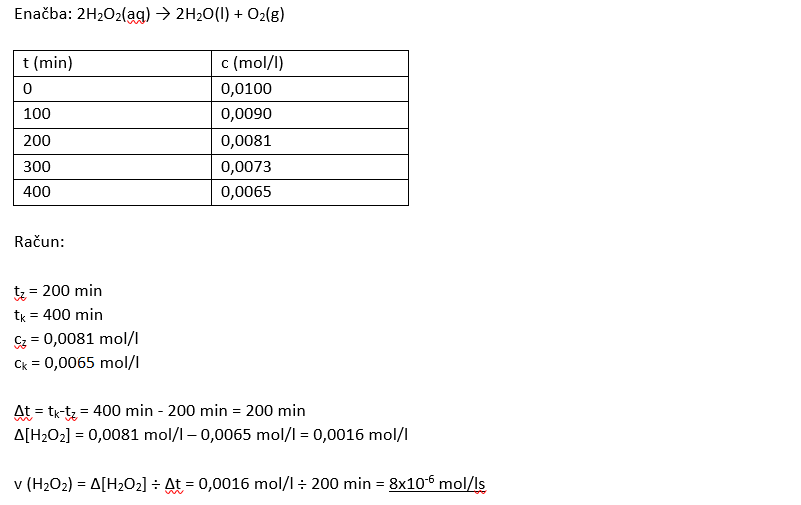
Primer 1: Izračunaj povprečno hitrost razpada vodikovega peroksida na kisik in vodo med v intervalu med 200. in 400. minuto. V tabeli so podane koncentracije vodikovega peroksida ori temperaturi 20°C.
Na hitrost reakcije lahko vplivamo na naslednje načine:
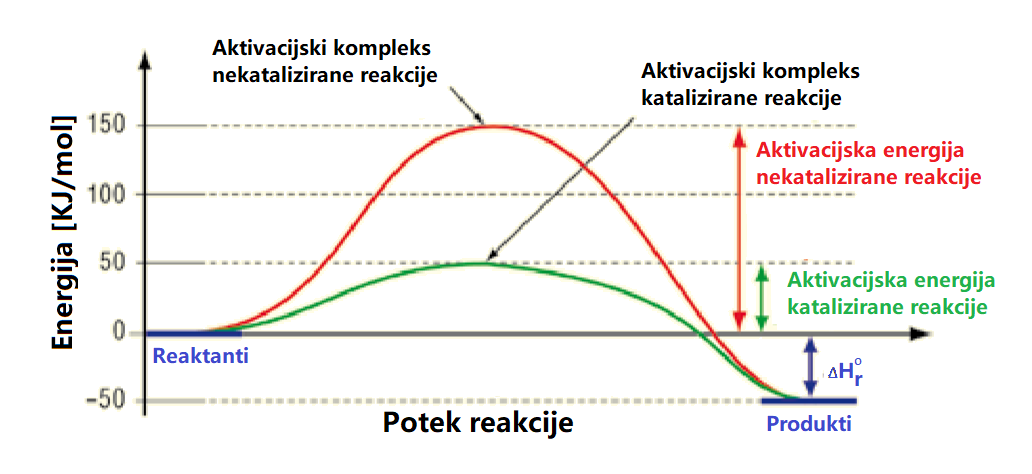
Slika prikazuje graf katalizirane in nekatalizirane reakcije. Rdeča krivulja predstavlja nekatalizirano, zelena pa katalizirano reakcijo. Vodoravna os predstavlja potek reakcije, navpična os pa energijo snovi. Katalizator spremeni hitrost reakcije na ta način, da zniža energijsko pregrado, kar je razvidno na grafu, kjer je zelena krivulja katalizirane reakcije nižja kot rdeča krivulja nekatalizirane. Stanje z največjo energijo, ki ga predstavlja vrh krivulje, imenujemo aktivacijsko ali prehodno stanje, molekularna struktura v tem stanju pa se imenuje aktivacijski kompleks. Iz tega lahko sklepamo, da je aktivacijska energija nekatalizirane reakcije večja od aktivacijske energije katalizirane reakcije. Aktivacijska energija je minimalna energija, ki je potrebna, da reaktanti dosežejo prehodno stanje in se nato pretvorijo v produkte.
Potrebujete dodatne informacije? Pomagajo vam lahko inštruktorji kemije.
kemija
Določite lokacijo
Določite termin
Dodatni filtri
Počisti
OŠ/SŠ
Študenti in ostali
Poišči mojo
lokacijo
Na domu
Online
Danes
(cena +50%)
Jutri
Jutri popoldne
Pojutrišnjem
Pojutrišnjem popoldne
Ta teden
Ta teden popoldne
V naslednjih treh dneh
V naslednjih treh dneh popoldne
Kadarkoli
Cena
Spol
Starost
Fakulteta
Razvrsti po:
Razvrsti po:


Zapri okno